Por Cristian García Martínez. Técnico de GanaSalud.
Introducción: ¿hasta qué punto está escrita nuestra salud?
Durante décadas, hablar de salud era hablar de herencia. Si alguien desarrollaba diabetes, hipertensión o problemas cardiovasculares, la explicación más habitual era sencilla: “lo lleva en los genes”. Esa idea no era errónea, pero sí incompleta. Hoy sabemos que entre lo que heredamos y lo que finalmente manifestamos existe una capa de regulación tan poderosa como silenciosa: la epigenética.
La epigenética no sustituye a la genética, ni la contradice. La completa. Nos permite entender por qué personas con una predisposición genética clara nunca desarrollan una enfermedad, mientras que otras, con una carga genética menor, sí lo hacen. También explica por qué el estilo de vida no actúa como un interruptor inmediato, sino como una fuerza acumulativa, lenta y profunda.
Este artículo no pretende vender soluciones mágicas ni culpabilizar a nadie, sino ofrecer una visión clara, honesta y científicamente respaldada de cómo nuestros hábitos dialogan con nuestros genes a lo largo del tiempo.
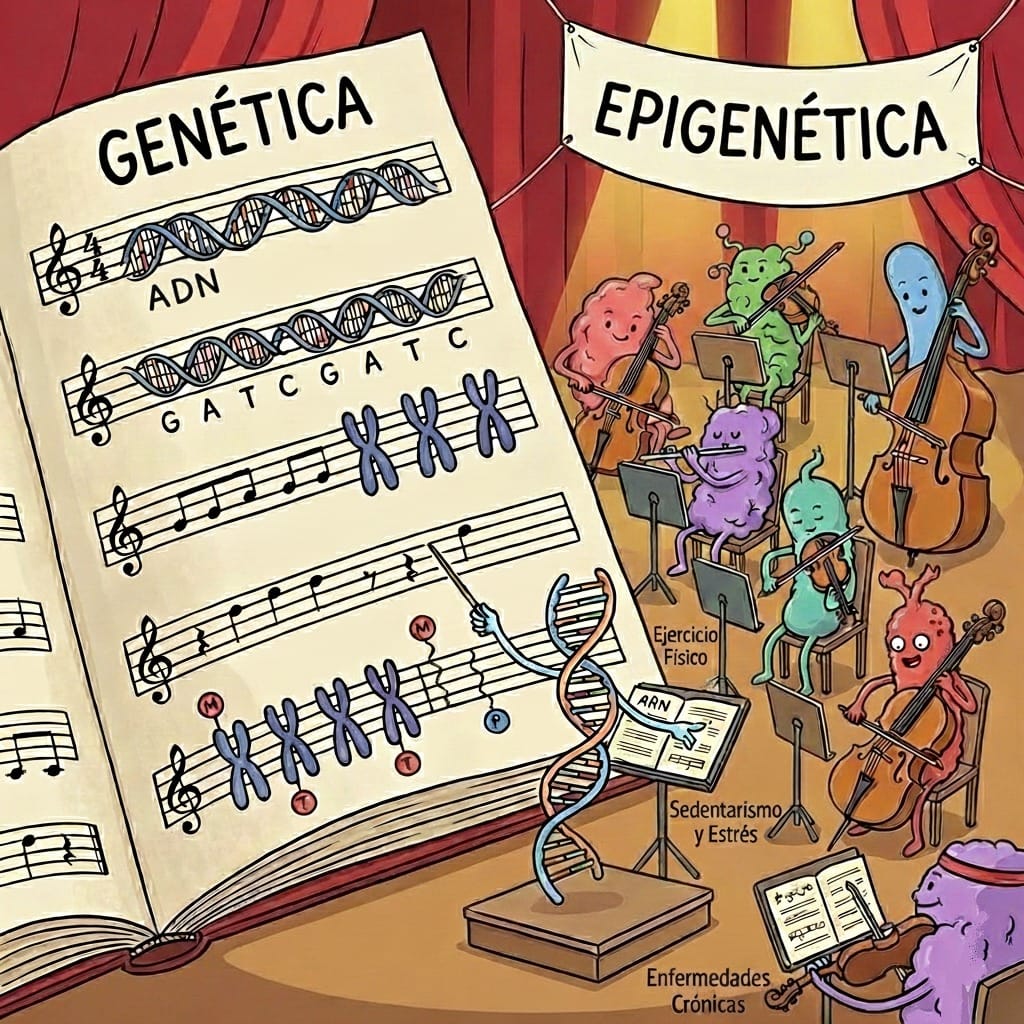
Genética y epigenética: la partitura y la interpretación
Para diferenciar genética y epigenética conviene recurrir a una metáfora sencilla. La genética es la partitura musical. En ella están escritas todas las notas desde el principio. No podemos cambiarla. Marca qué melodías son posibles y cuáles no. La epigenética, en cambio, es el músico y el director de la orquesta. Decide cómo se interpreta esa partitura: el ritmo, la intensidad, los silencios, qué instrumentos destacan y cuáles pasan a un segundo plano.
Dos orquestas con la misma partitura pueden generar músicas completamente distintas. Del mismo modo, dos personas con genes muy similares pueden tener estados de salud radicalmente diferentes. La epigenética no altera el texto genético, pero sí determina qué genes se expresan, cuándo y durante cuánto tiempo.
Esto no significa que todo esté bajo nuestro control. La genética impone límites reales. Pero dentro de esos límites existe un margen de adaptación mucho mayor del que se pensaba hace solo unas décadas.
¿Qué es realmente la epigenética?
Desde un punto de vista biológico, la epigenética estudia los mecanismos que regulan la expresión de los genes sin modificar la secuencia del ADN. Dicho de forma más simple: el texto no cambia, pero sí la forma en la que se lee.
Estos mecanismos responden al entorno y a los hábitos cotidianos. La alimentación, el ejercicio, el descanso, el estrés, las emociones mantenidas en el tiempo o la exposición a sustancias químicas envían señales constantes a nuestras células. La epigenética es la forma en la que el cuerpo traduce esas señales en cambios funcionales.
Es importante entender que estos cambios no suelen ser inmediatos. La epigenética funciona como un registro histórico de cómo vivimos. Por eso resulta tan relevante en enfermedades crónicas y procesos de envejecimiento.
Los tres grandes mecanismos epigenéticos
Metilación del ADN: el libro de recetas que no siempre se cocina
Imaginemos el ADN como un enorme libro de recetas. Todas las recetas están ahí desde el principio, pero no todas se utilizan. La metilación del ADN actúa como pequeñas marcas que cubren determinadas páginas. Cuando una receta está tapada, no se lee; cuando se destapa, puede cocinarse.
En términos biológicos, la metilación suele reducir la expresión de un gen. Este mecanismo es esencial para el desarrollo normal y la especialización celular, pero cuando los patrones de metilación se alteran de forma crónica, pueden aparecer problemas. Algunos patrones se han asociado a inflamación persistente, resistencia a la insulina, alteraciones metabólicas y envejecimiento acelerado. Digamos que en ese libro de cocina, si estás buscando una receta de merluza a la plancha y te aparece en blanco esa hoja, o incluso te aparece la receta de otro plato, no tendríamos muy buenos resultados para nada.
Conviene insistir en un punto clave: no existe una “metilación buena” o “mala” universal. Lo importante es el equilibrio del conjunto, no un gen aislado.
Histonas: el texto enrollado que no se puede leer
El ADN no flota libremente en la célula, sino que está enrollado alrededor de proteínas llamadas histonas. Podemos imaginarlo como un texto escrito en una tela que puede estar tan enrollada que resulta ilegible, solo se puede leer si se desenrolla lo suficiente.
Cuando el ADN está muy compacto, los genes quedan inaccesibles. Cuando se relaja, pueden expresarse. Factores como el ejercicio físico regular, el descanso adecuado y una nutrición equilibrada favorecen configuraciones más “legibles”. Por el contrario, el estrés crónico, la falta de sueño o el sedentarismo tienden a favorecer un enrollamiento menos efectivo, dificultado la lectura de ciertos genes cuando se necesitan en un momento concreto, produciendo más problemas a largo plazo …
ARN no codificante: el agente de tráfico genético
Durante años se pensó que el ARN solo servía para fabricar proteínas. Hoy sabemos que una gran parte del ARN no codifica proteínas, sino que regula el sistema. Funciona como un agente de tráfico, indicando qué genes pueden expresarse, cuáles deben detenerse y en qué momento hacerlo.
Estos ARN no codificantes, por ejemplo, responden de forma muy sensible a estímulos como el ejercicio, la inflamación o el estrés. Su desregulación se ha relacionado con enfermedades cardiovasculares, metabólicas y neurodegenerativas. Son discretos, pero imprescindibles para mantener el orden.
El ejercicio físico: uno de los grandes protagonistas epigenéticos
Desde una perspectiva evolutiva, el movimiento no es opcional. Nuestros genes esperan actividad física, el ser humano dependía de sus habilidades físicas y cognitivas en un mundo de supervivencia. El ejercicio actúa como una señal epigenética potente capaz de modificar patrones de metilación, regular histonas y ajustar la expresión de ARN no codificante en tejidos clave como el músculo, el hígado, el cerebro, venas, arterias y el resto del cuerpo.
No hablamos de entrenamientos extremos ni de rendimiento deportivo. Caminar, entrenar fuerza, moverse con regularidad ya genera adaptaciones epigenéticas positivas. Eso sí, conviene evitar el mensaje simplista de que “más siempre es mejor”. El ejercicio excesivo, mal programado o sin recuperación suficiente también puede actuar como un estresor negativo, “afortunadamente”, la gran mayoría de la población está muy alejado de ese punto y desafortunadamente muy pocos llegan al mínimo recomendado, dificultando la expresión correcta de sus genes en base a lo que esperan.
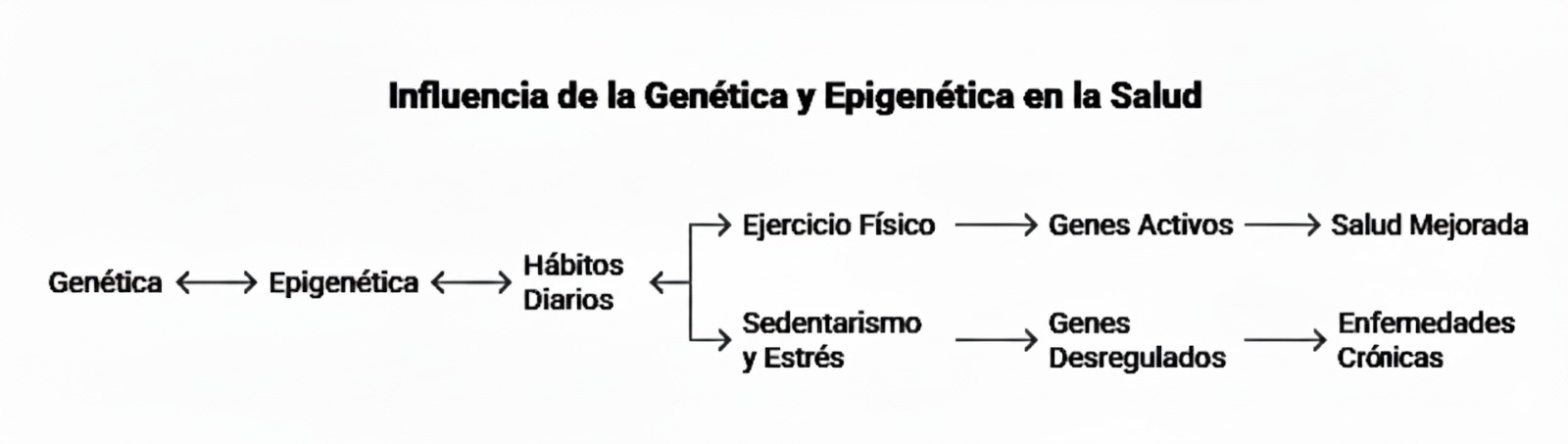
Los hábitos diarios: la gota de agua sobre la piedra
La epigenética no responde a gestos heroicos aislados, sino a la repetición. Es como una gota de agua cayendo sobre una piedra. Una sola gota no hace nada. Miles, con el tiempo, dejan huella.
Dormir mal una noche no enferma a nadie. Dormir mal durante años, sí. Comer de forma desequilibrada un día no altera la biología. Hacerlo de forma crónica, sí. La epigenética explica por qué las enfermedades crónicas no aparecen de repente, sino tras años de pequeñas decisiones acumuladas. La hipertensión a los 55 ya empezó hace 20 o 30 años, en la mayoría de los casos, y así mismo con otras patologías como diabetes tipo II y la resistencia a la insulina, los vasos sanguíneos alterados, etc.
Por qué no deberíamos normalizar las enfermedades crónicas “habituales”
Hipertensión, diabetes tipo II o perfiles alterados de colesterol son frecuentes, pero no normales desde un punto de vista biológico. Muchas comparten patrones epigenéticos relacionados con inflamación de bajo grado, disfunción metabólica y estrés mantenido.
Normalizarlas reduce la percepción de reversibilidad y refuerza un enfoque exclusivamente farmacológico. Entender la epigenética no culpabiliza al individuo, pero sí amplía el foco hacia las causas profundas, se mira la raíz del problema.
Emociones y regulación epigenética
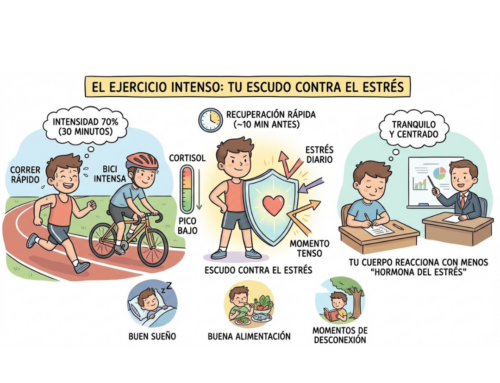
Por otro lado, el cuerpo no distingue entre estrés psicológico y físico. El cerebro no distingue si estamos huyendo de un león hambriento o de un tráfico agobiante en medio de la ciudad. Ambos activan respuestas hormonales reales, el cortisol, con una gran función evolutiva que nos permitió sobrevivir, sin embargo, de forma sostenida este estrés no tiene ninguna función útil, una alarma siempre encendida solo agota todos los recursos de defensa, y cuando estos haga falta de verdad el organismo estará mermado, afectando a la memoria, al sistema inmune, etc.
El estrés crónico, el miedo o la ira sostenida elevan de forma persistente el cortisol y otros mediadores inflamatorios que influyen en la regulación epigenética.
En el otro extremo, estados de calma, seguridad, gratitud o vínculo social se asocian a perfiles hormonales más estables. No se trata de “pensar en positivo”, sino de reconocer que las emociones mantenidas tienen efectos fisiológicos acumulativos.
Además las respiraciones conscientes o la meditación, incluso una buena filosofía de vida, pueden ayudar a esta regulación positiva de las emociones.
Algunas conclusiones
Muchos términos e información nueva, próximamente habrá otro artículo como continuación de este donde se mencionará también los cambios epigenéticos a partir de nuestra microbiota y de los tóxicos que nos rodean que muchas veces no tenemos en cuenta entre otros temas.
Pero hasta ahora debemos quedarnos con que no todo depende de la suerte o la mala suerte, que no depende de momentos puntuales de buenos hábitos o malos hábitos, sino que lo importante es cómo esa gota moldea la roca a base de repetición en el tiempo, eso es lo importante, el saber que aunque haya una “partitura musical” nosotros somos quienes la interpretan y la llevan a cabo, no podemos editarla o cambiarla, pero somos nosotros quien la ejecuta de una forma u otra gracias a nuestro estilo de vida y hábitos.
Referencias bibliográficas
- Baladia, E., Moñino, M., Pleguezuelos, E., Russolillo, G., & Garnacho-Castaño, M. V. (2024). Broccoli Consumption and Risk of Cancer: An Updated Systematic Review and Meta-Analysis of Observational Studies. Nutrients, 16(11), 1583. https://doi.org/10.3390/nu16111583
- Carvajal, A. (2005). Estrés y depresión: una mirada desde la clínica a la neurobiología. Revista Médica Clínica Las Condes, 16(4).
- Donga, E., van Dijk, M., van Dijk, J. G., Biermasz, N. R., Lammers, G. J., van Kralingen, K. W., Corssmit, E. P., & Romijn, J. A. (2010). A single night of partial sleep deprivation induces insulin resistance in multiple metabolic pathways in healthy subjects. The Journal of clinical endocrinology and metabolism, 95(6), 2963–2968. https://doi.org/10.1210/jc.2009-2430
- Möller-Levet, C. S., Archer, S. N., Bucca, G., Laing, E. E., Slak, A., Kabiljo, R., Lo, J. C., Santhi, N., von Schantz, M., Smith, C. P., & Dijk, D. J. (2013). Effects of insufficient sleep on circadian rhythmicity and expression amplitude of the human blood transcriptome. Proceedings of the National Academy of Sciences of the United States of America, 110(12), E1132–E1141. https://doi.org/10.1073/pnas.1217154110
- Pascoe, M. C., Thompson, D. R., Jenkins, Z. M., & Ski, C. F. (2017). Mindfulness mediates the physiological markers of stress: Systematic review and meta-analysis. Journal of psychiatric research, 95, 156–178. https://doi.org/10.1016/j.jpsychires.2017.08.004
- Qureshi, I. A., & Mehler, M. F. (2014). Epigenetics of sleep and chronobiology. Current neurology and neuroscience reports, 14(3), 432. https://doi.org/10.1007/s11910-013-0432-6
- Sharma, V. K., & Singh, T. G. (2020). Chronic Stress and Diabetes Mellitus: Interwoven Pathologies. Current diabetes reviews, 16(6), 546–556. https://doi.org/10.2174/1573399815666191111152248





Enhorabuena.Me ha parecido muy interesante, bien explicado.